
-
 Spanische Justiz gibt Fall Fernandes gegen Ulmen an deutsche Behörden ab
Spanische Justiz gibt Fall Fernandes gegen Ulmen an deutsche Behörden ab
-
US-Vizepräsident Vance: Der Iran ist bei Friedensverhandlungen am Zug

-
 Gutachter: Deutschlandticket nutzt Umwelt, Wirtschaft und Verbrauchern
Gutachter: Deutschlandticket nutzt Umwelt, Wirtschaft und Verbrauchern
-
Außenminister: Israel will "Frieden und Normalisierung" mit Libanon

-
 Dröge fordert wegen Energiekrise Stromsteuersenkung und Tempolimit
Dröge fordert wegen Energiekrise Stromsteuersenkung und Tempolimit
-
Kiew und Berlin erweitern Beziehungen zu neuer Strategischer Partnerschaft

-
 Ökonom Feld fordert rigorosen Abbau staatlicher Subventionen
Ökonom Feld fordert rigorosen Abbau staatlicher Subventionen
-
Streiks bei der Lufthansa sorgen auch am Dienstag für zahlreiche Flugausfälle

-
 Xi zum Iran-Krieg: China wird "konstruktive Rolle" bei Friedensbemühungen spielen
Xi zum Iran-Krieg: China wird "konstruktive Rolle" bei Friedensbemühungen spielen
-
Kiew und Berlin beschließen Kooperationen bei Verteidigung und Wiederaufbau

-
 Straße von Hormus: Paris und London planen Videokonferenz am Freitag
Straße von Hormus: Paris und London planen Videokonferenz am Freitag
-
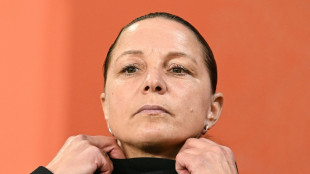
Pionierin Grings: Sexismus nur von "Schwachköpfen"
-
 Bundesamt warnt vor Sturmflutrisiken - Aufbau störungssicherer Navigationssysteme
Bundesamt warnt vor Sturmflutrisiken - Aufbau störungssicherer Navigationssysteme
-
Tötung von Kollegin aus Mordlust: Lebenslange Haft für Mann in Schweinfurt

-
 Dobrindt eröffnet Beratungszentrum für Ukrainer in Berlin
Dobrindt eröffnet Beratungszentrum für Ukrainer in Berlin
-
Eta leitet erste Einheit als Union-Cheftrainerin

-
 Kimmich appelliert an Fans: "Wir brauchen euch!"
Kimmich appelliert an Fans: "Wir brauchen euch!"
-
Grüne und CDU in Baden-Württemberg wollen Koalitionsverhandlungen aufnehmen

-
 "Glasfasermord" an Vorarbeiter im Saarland: Urteil gegen vier Täter rechtskräftig
"Glasfasermord" an Vorarbeiter im Saarland: Urteil gegen vier Täter rechtskräftig
-
IEA: Stärkster Einbruch der Ölnachfrage seit Corona-Pandemie

-
 Frankreichs Außenminister: Putin verliert mit Orban sein "trojanisches Pferd"
Frankreichs Außenminister: Putin verliert mit Orban sein "trojanisches Pferd"
-
Vergewaltigungsvorwürfe und Affäre: Zwei US-Kongressabgeordnete verkünden Rücktritt

-
 Regionalliga: Bayern lehnt Reformvorschläge ab
Regionalliga: Bayern lehnt Reformvorschläge ab
-
Bund greift verschuldeten Kommunen unter die Arme - Gesetz am Mittwoch im Kabinett

-
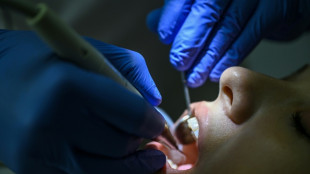 Gesundheitsstudie: Großteil der Kinder in Deutschland ist kariesfrei
Gesundheitsstudie: Großteil der Kinder in Deutschland ist kariesfrei
-
Nachwahlen in Kanada: Premier Carney verfügt nun über absolute Mehrheit

-
 CDU-Generalsekretär Linnemann fordert Abschaffung der meisten Krankenkassen
CDU-Generalsekretär Linnemann fordert Abschaffung der meisten Krankenkassen
-
Zahl neuer Ausbildungsverträge 2025 erneut rückläufig

-
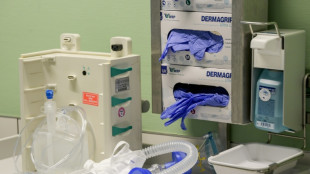 Umfrage: Machtmissbrauch und sexuelle Belästigung in Kliniken großes Problem
Umfrage: Machtmissbrauch und sexuelle Belästigung in Kliniken großes Problem
-
Langer Streit um Schnipsel aus Stück von Kraftwerk: Bundesgerichtshof wieder am Zug

-
 Oasis und Phil Collins werden in Rock and Roll Hall of Fame aufgenommen
Oasis und Phil Collins werden in Rock and Roll Hall of Fame aufgenommen
-
Filmstars wenden sich in offenem Brief gegen Warner-Bros.-Übernahme durch Paramount

-
 Zahl der in Deutschland an Folgen von Zeckenstich gestorbenen Menschen steigt
Zahl der in Deutschland an Folgen von Zeckenstich gestorbenen Menschen steigt
-
Importabhängigkeit bei Seltenen Erden aus China etwas zurückgegangen

-
 Merz empfängt Selenskyj zu deutsch-ukrainischen Konsultationen
Merz empfängt Selenskyj zu deutsch-ukrainischen Konsultationen
-
Kretschmer kritisiert Koalitionsbeschlüsse scharf: 1000-Euro-Entlastung "Hohn"

-
 Spritpreiskrise: 51 Prozent der Deutschen für zeitlich begrenztes Tempolimit
Spritpreiskrise: 51 Prozent der Deutschen für zeitlich begrenztes Tempolimit
-
Kabelschaden legt Gelsenkirchener Hauptbahnhof lahm - Polizei prüft Sabotage

-
 Chinas Exporte schwächeln - Importe wegen hoher Energiepreise im März gestiegen
Chinas Exporte schwächeln - Importe wegen hoher Energiepreise im März gestiegen
-
Prinz Harry und Meghan in Australien - Erster Besuch seit Bruch mit Königshaus

-
 Kurz vor Playoff-Start: Draisaitl zurück auf dem Eis
Kurz vor Playoff-Start: Draisaitl zurück auf dem Eis
-
Russischer Außenminister zu Gesprächen über Iran-Krieg in China

-
 Kanada: Partei von Premier Carney sichert sich in Nachwahlen Mehrheit im Parlament
Kanada: Partei von Premier Carney sichert sich in Nachwahlen Mehrheit im Parlament
-
Teheran: US-Teilblockade der Straße von Hormus verletzt Souveränität des Iran

-
 WNBA-Draft: Bühner als Nummer 17 nach Portland
WNBA-Draft: Bühner als Nummer 17 nach Portland
-
Staatsmedien: Nordkorea feuert Raketen von Marinezerstörer ab

-
 Gwinn über WM-Quali: "Die eigene Identität stärken"
Gwinn über WM-Quali: "Die eigene Identität stärken"
-
Reiter erwartet "steinigen" Weg zurück an die Weltspitze

-
 Figo schwärmt von Olise: "Ich liebe ihn"
Figo schwärmt von Olise: "Ich liebe ihn"
-
US-Vize Vance: Vatikan sollte sich "auf moralische Fragen beschränken"


BioNxt beginnt mit der GMP-konformen Herstellung eines sublingualen Cladribin-Films in klinischer Qualität zur Behandlung von Multipler Sklerose (MS)
VANCOUVER, BC / ACCESS Newswire / 14. April 2026 / BioNxt Solutions Inc. („BioNxt" oder das „Unternehmen") (CSE:BNXT)(OTCQB:BNXTF)(FWB:BXT), ein innovatives Biowissenschaftsunternehmen, das sich auf fortschrittliche Systeme zur Verabreichung von Medikamenten spezialisiert hat, freut sich, den erfolgreichen Abschluss der Herstellung seines sublingualen Cladribin-Dünnfilms (ODF) in klinischer Qualität nach den Grundsätzen der Guten Herstellungspraxis (GMP) bei seinem GMP-Produktionspartner (CDMO) mit Sitz in München bekannt zu geben.
Die abgeschlossene GMP-Produktionskampagne stellt einen bedeutenden operativen Meilenstein für das führende Entwicklungsprogramm von BioNxt dar. BNT23001 ist eine proprietäre sublinguale Cladribin-Formulierung, die für die Behandlung von schubförmiger Multipler Sklerose (MS) und anderen autoimmunen neurodegenerativen Erkrankungen entwickelt wurde. Mit diesem Erfolg schreitet das Unternehmen von der Formulierungsentwicklung und präklinischen Validierung zur vollständigen Durchführung der klinischen Phase voran.
Bereitschaft für die klinische Phase und Vorbereitung der klinischen Studie
Die beim GMP-Produktionspartner (CDMO) von BioNxt mit Sitz in München, Deutschland, hergestellte GMP-Charge wird als Prüfpräparat (IMP) für die geplante Studie zur Bioverfügbarkeit am Menschen von BioNxt dienen. CBN26001 ist eine offene, randomisierte Crossover-Studie mit zwei Phasen, in der das sublinguale Cladribin-ODF des Unternehmens mit dem Referenzprodukt Mavenclad® (orale Cladribin-Tabletten) verglichen werden soll.
Die Herstellung erfolgte gemäß den GMP-Standards der Europäischen Union, einschließlich validierter Produktionsprozesse, kontrollierter Rohstoffbeschaffung, umfassender Prozesskontrollen sowie vollständiger Qualitätsprüfungen und -dokumentation zur Vorbereitung der Freigabe durch einen qualifizierten Sachverständigen und der klinischen Anwendung. Außerdem wurden Stabilitätsstudien eingeleitet.
Der Abschluss der GMP-konformen Herstellung markiert den letzten technischen Schritt vor dem Start der klinischen Studie und versetzt BioNxt in die Lage, die erste Verabreichung an Menschen für seine proprietäre ODF-Formulierung durchzuführen. Dieser Erfolg reduziert das operative Risiko im Cladribin-Programm erheblich und stärkt die regulatorische Bereitschaft des Unternehmens, während es sich auf den Eintritt in die klinische Phase am Menschen vorbereitet.
Validierung der Plattform und strategische Expansion
Das sublinguale Cladribin-ODF von BioNxt wurde entwickelt, um die wesentlichen Einschränkungen der herkömmlichen oralen Verabreichung zu überwinden, darunter Schwankungen bei der gastrointestinalen Resorption, der Abbau unter sauren Magenbedingungen, transporterbedingten Efflux im oberen Darm sowie Schluckbeschwerden, die bei MS-Patienten häufig auftreten. Durch die Ermöglichung einer transmukosalen Resorption mittels eines sich schnell auflösenden, nadelfreien sublingualen Films strebt das Unternehmen an, eine patientenfreundliche Alternative anzubieten, die eine verbesserte Compliance und eine besser vorhersagbare systemische Exposition ermöglichen könnte.
Die Zusammenarbeit mit der europäischen GMP-zertifizierten Auftragsentwicklungs- und Produktionsorganisation (CDMO) von BioNxt verschafft dem Unternehmen eine skalierbare und den regulatorischen Anforderungen entsprechende Produktionsinfrastruktur, die zukünftige Zulassungsstudien und eine potenzielle Produktion im kommerziellen Maßstab unterstützen kann. Der etablierte Prozess ist darauf ausgelegt, einen effizienten Technologietransfer für regionale Lizenz- oder Co-Entwicklungspartnerschaften zu ermöglichen, insbesondere in europäischen Märkten, in denen BioNxt kürzlich sein Portfolio an geistigem Eigentum ausgebaut hat. Der Abschluss der GMP-Herstellung unterstützt nicht nur die geplante klinische Studie, sondern stärkt auch die Position des Unternehmens in strategischen Partnerschaftsgesprächen, indem er die technische Bereitschaft und die Fähigkeit zur regulatorischen Umsetzung demonstriert.
„Der Abschluss der GMP-Herstellung unseres Cladribin-ODF in klinischer Qualität ist ein entscheidender Meilenstein für BioNxt", sagte Hugh Rogers, Chief Executive Officer von BioNxt Solutions Inc. „Diese Errungenschaft demonstriert unsere Fähigkeit, innovative Formulierungswissenschaft in regulatorisch zulassungsfähige klinische Produkte umzusetzen, und bringt uns der Generierung von Daten aus Humanstudien näher. Wir glauben, dass dieser Meilenstein unsere Strategie, BioNxt als führendes Unternehmen im Bereich der nadelfreien Arzneimittelverabreichungssysteme der nächsten Generation zu positionieren, erheblich vorantreibt."
Das Unternehmen geht davon aus, zu gegebener Zeit weitere Informationen zur Einleitung der klinischen Studie und zur ersten Verabreichung an Probanden bekannt zu geben.
Über BioNxt Solutions Inc.
BioNxt Solutions Inc. ist ein innovatives Biowissenschaftsunternehmen, das sich auf Plattformen für die Verabreichung von Medikamenten der nächsten Generation, diagnostische Screening-Systeme und die Entwicklung pharmazeutischer Wirkstoffe konzentriert. Zu seinen proprietären Plattformen gehören sublinguale Dünnfilme, transdermale Pflaster, orale Tabletten und eine neue Plattform für gezielte Chemotherapie, die Krebsmedikamente direkt an Tumore abgibt und gleichzeitig Nebenwirkungen reduziert.
Mit seinen Forschungs- und Entwicklungsaktivitäten in Nordamerika und Europa erzielt BioNxt entsprechende Fortschritte bei den behördlichen Zulassungsverfahren und Vermarktungsinitiativen, wobei der Fokus in erster Linie auf den europäischen Märkten liegt. BioNxt hat sich zum Ziel gesetzt, die Gesundheitsversorgung durch die Bereitstellung von präzisen, patientenzentrierten Lösungen zu verbessern, mit denen man weltweit größere Behandlungserfolge erzielen will.
BioNxt notiert an der Canadian Securities Exchange (BNXT), im OTC-Markt (BNXTF) und in Deutschland (WKN: A3D1K3). Nähere Informationen zu BioNxt erhalten Sie unter www.bionxt.com.
Investor Relations und Medien
Hugh Rogers, Mitbegründer, CEO und Vorstandsmitglied
E-Mail: [email protected]
Telefon: +1 780-818-6422
Web: www.bionxt.com
LinkedIn: https://www.linkedin.com/company/bionxt-solutions
Instagram: https://www.instagram.com/bionxt
Warnhinweis zu „zukunftsgerichteten" Informationen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen im Sinne der geltenden Wertpapiergesetze. Zukunftsgerichtete Aussagen basieren auf den aktuellen Erwartungen, Schätzungen, Prognosen, Überzeugungen und Annahmen des Managements zum Zeitpunkt dieser Veröffentlichung.
Zu den zukunftsgerichteten Aussagen in dieser Mitteilung gehören unter anderem Aussagen bezüglich: der Verhandlung und möglichen Unterzeichnung einer endgültigen Lizenzvereinbarung gemäß der unverbindlichen Absichtserklärung; des Umfangs, der territorialen Abdeckung, der Gültigkeit, der Laufzeit und der Durchsetzbarkeit des eurasischen Patents des Unternehmens; der Strategie des Unternehmens im Bereich des geistigen Eigentums; der weiteren Entwicklung seines Programms für sublinguale Cladribin-Oral-Thin-Film-Präparate (ODF); des voraussichtlichen Zeitplans, die Konzeption und die Durchführung geplanter Bioäquivalenzstudien am Menschen; potenzieller Zulassungswege; der Ausweitung auf weitere Indikationen; sowie potenzieller Kommerzialisierungs-, Lizenzierungs- oder Partnerschaftsaktivitäten.
Zukunftsgerichtete Aussagen unterliegen bekannten und unbekannten Risiken, Ungewissheiten und anderen Faktoren, die dazu führen können, dass die tatsächlichen Ergebnisse, Leistungen oder Erfolge wesentlich von den in solchen zukunftsgerichteten Aussagen ausgedrückten oder implizierten Ergebnissen abweichen. Zu diesen Risiken und Ungewissheiten zählen unter anderem: die Möglichkeit, dass eine endgültige Vereinbarung nicht innerhalb der Exklusivitätsfrist oder überhaupt nicht zustande kommt; Risiken im Zusammenhang mit dem Schutz und der Durchsetzung geistigen Eigentums; potenzielle Patentwidersprüche oder Anfechtungen der Gültigkeit; Ungewissheiten hinsichtlich der behördlichen Prüfung und Zulassung; wissenschaftliche, formulierungsbezogene und entwicklungsbezogene Risiken; die Möglichkeit, dass präklinische oder pharmakokinetische Ergebnisse keine Vorhersagen über klinische Ergebnisse beim Menschen zulassen; Risiken im Zusammenhang mit dem Zeitplan, den Kosten und den Ergebnissen von Studien; Risiken bei der Herstellung und der Skalierung; die Abhängigkeit von externen Dienstleistern; Wettbewerbsentwicklungen; geopolitische Risiken in der eurasischen Region; sowie allgemeine wirtschaftliche, Markt- und Kapitalmarktbedingungen.
Leser werden darauf hingewiesen, sich nicht übermäßig auf zukunftsgerichtete Aussagen zu verlassen. Sofern nicht durch geltende Wertpapiergesetze vorgeschrieben, übernimmt BioNxt keine Verpflichtung, zukunftsgerichtete Aussagen zu aktualisieren oder zu revidieren, um neuen Informationen, zukünftigen Ereignissen oder sonstigen Umständen Rechnung zu tragen.
Mavenclad® ist eine eingetragene Marke, die nicht Eigentum von BioNxt Solutions Inc. ist und mit diesem Unternehmen weder verbunden noch von ihm gesponsert oder assoziiert ist.
QUELLE: BioNxt Solutions Inc.
G.P.Martin--AT

